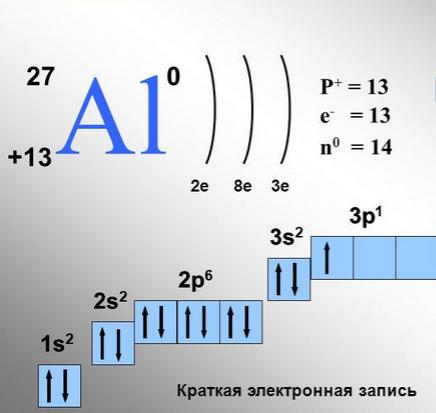
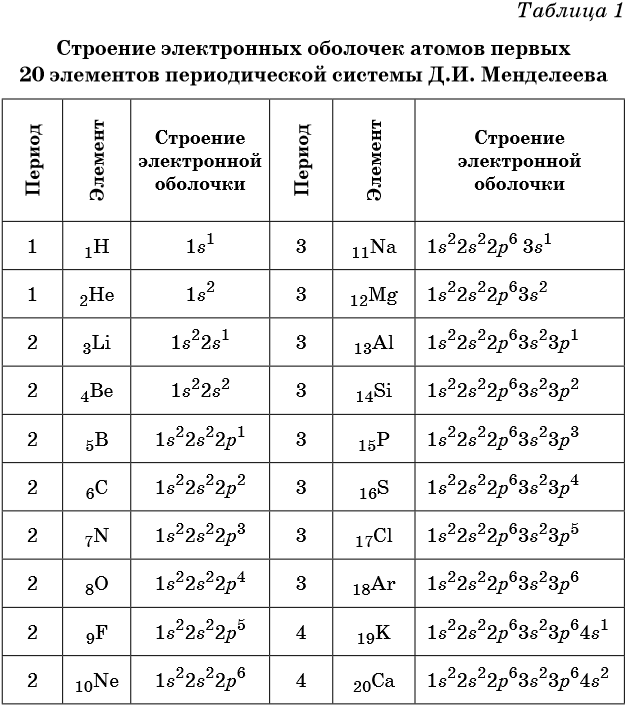
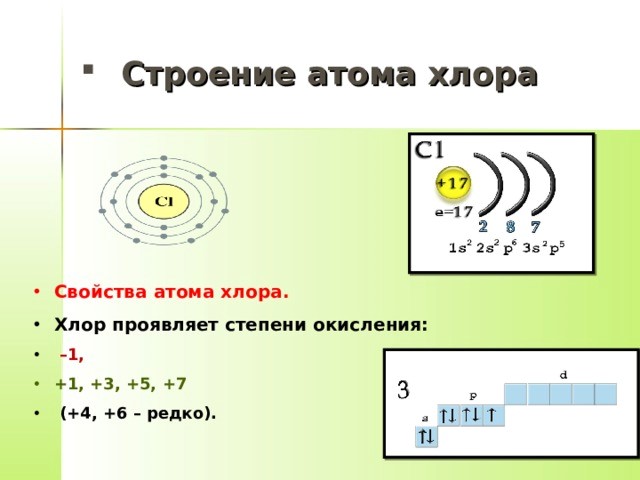
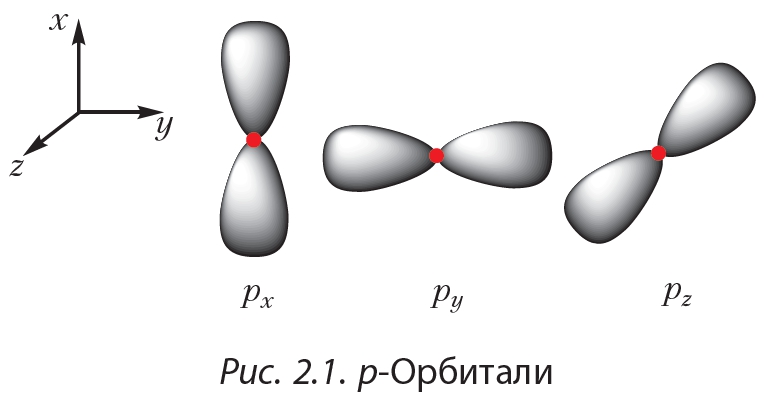
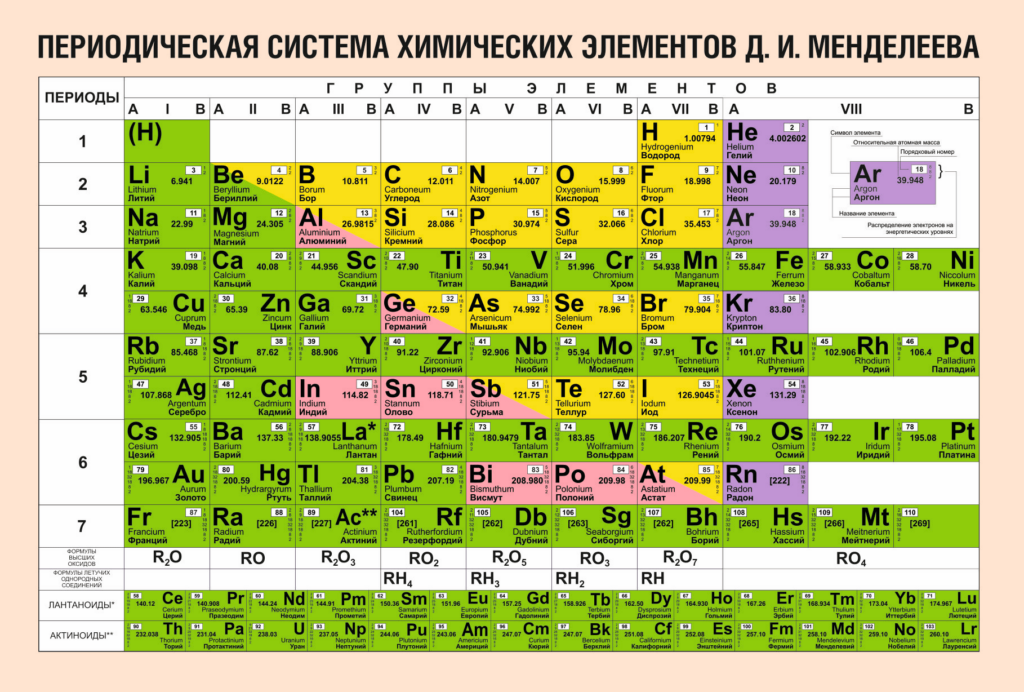
Электронная оболочка атома
Разноуровневый урок химии в 8 классе по теме "Строение электронных оболочек атомов" по программе О. Габриеляна позволяет на практике реализовать ЛО подход в обучении. Углубить знания о взаимосвязи строения атома и структурой ПСХЭ; 2.
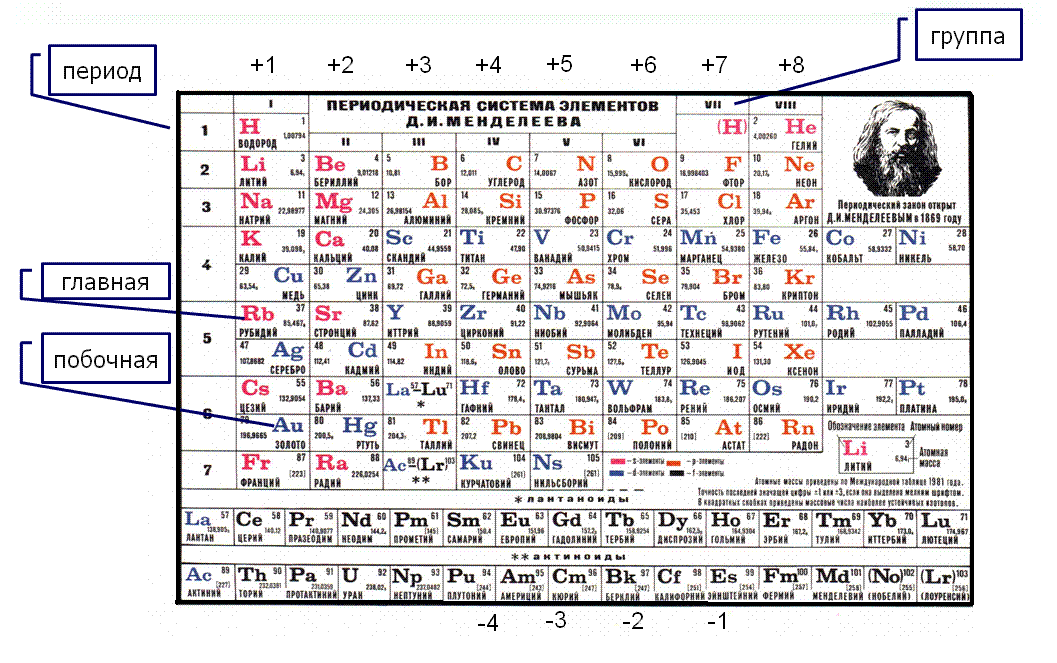
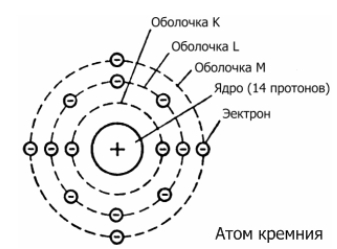

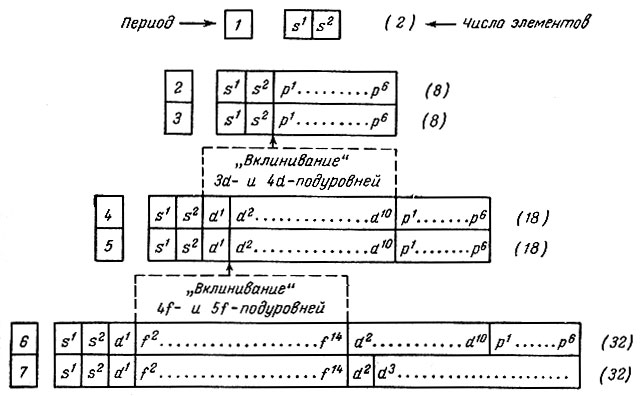
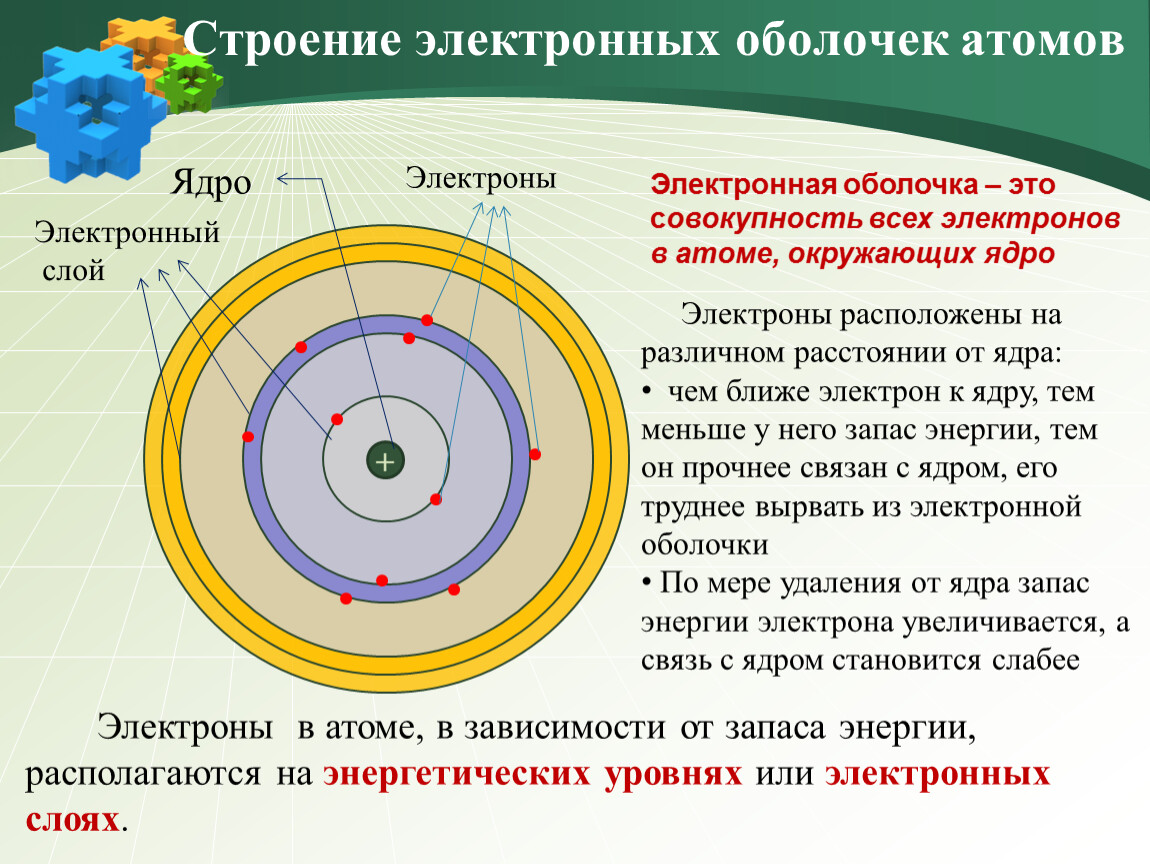

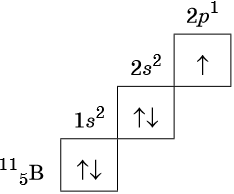
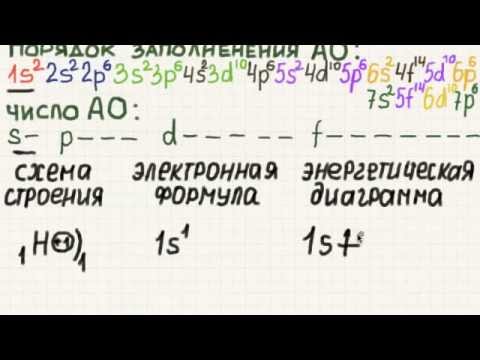
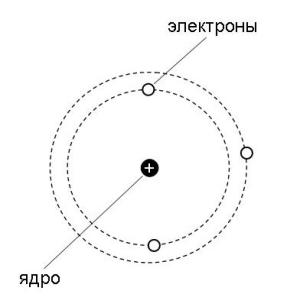
В химических реакциях ядра атомов не изменяются. Было установлено, что все химические свойства веществ определяются строением электронных оболочек атомов. Благодаря необычайно малой массе электрон обладает свойствами не только частицы, но и волны, т. Как частица электрон имеет определённую массу и заряд, а движущиеся электроны проявляют волновые свойства, например, поток электронов способен к дифракции, т. Проявляя волновые свойства, электрон, может в одно и то же время находиться в разных точках пространства, поэтому электрон представляет собой не точку, а электронное облако. Электронные облака, создаваемые отдельными электронами, в сумме создают электронную оболочку атома.
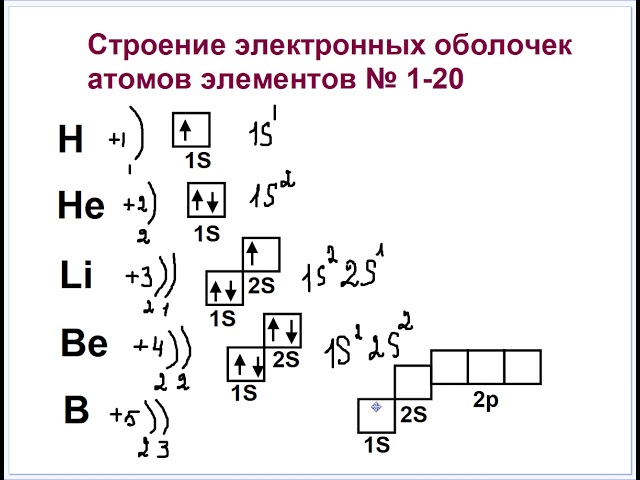
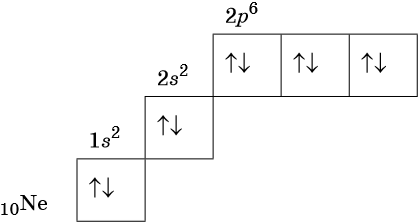
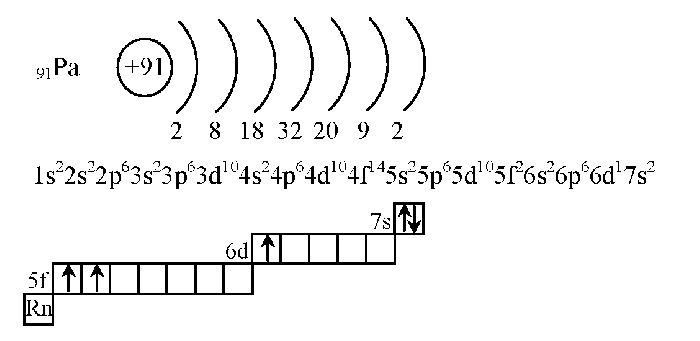
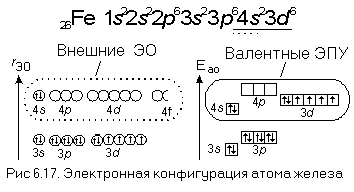



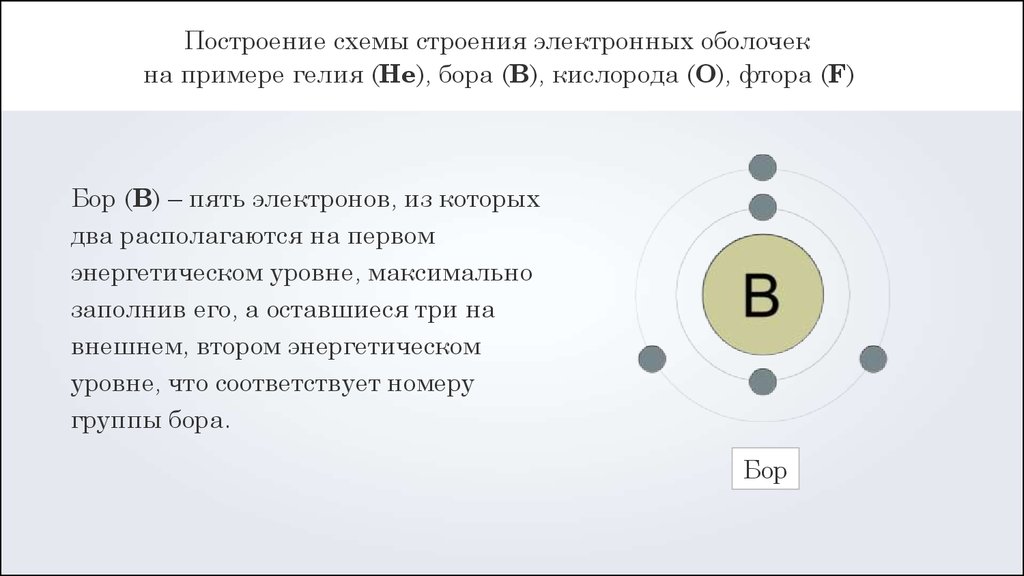
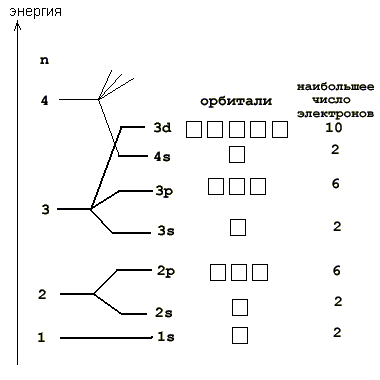
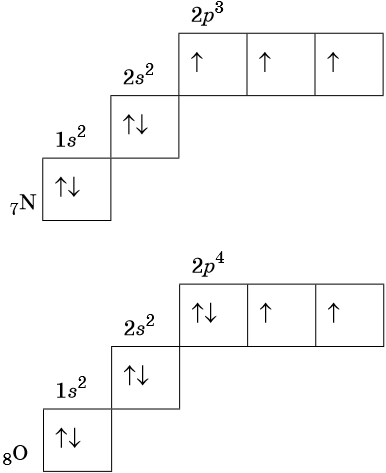
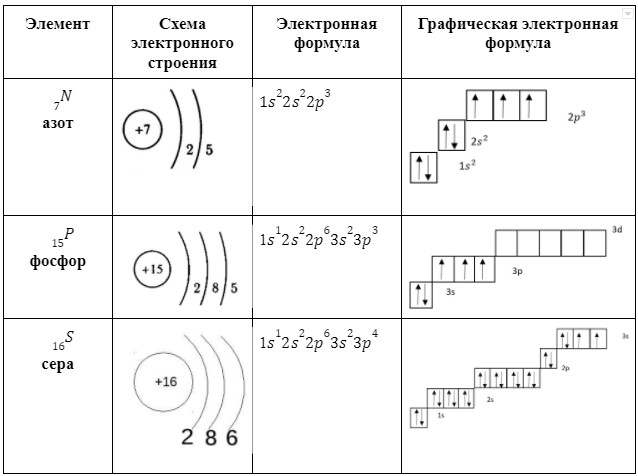
Главная страница » Химия » 8 класс » Основы химии » Атомы химических элементов » Строение атома: электронные формулы, электронные орбитали. На предыдущем уроке вы познакомились с первой частью темы о строении электронных оболочек. Вы узнали, что собой представляют электронные оболочки атомов, что такое электронные слои и как они заполняются. Данный урок представляет вторую часть темы о строении электронных оболочек.